Covid-19
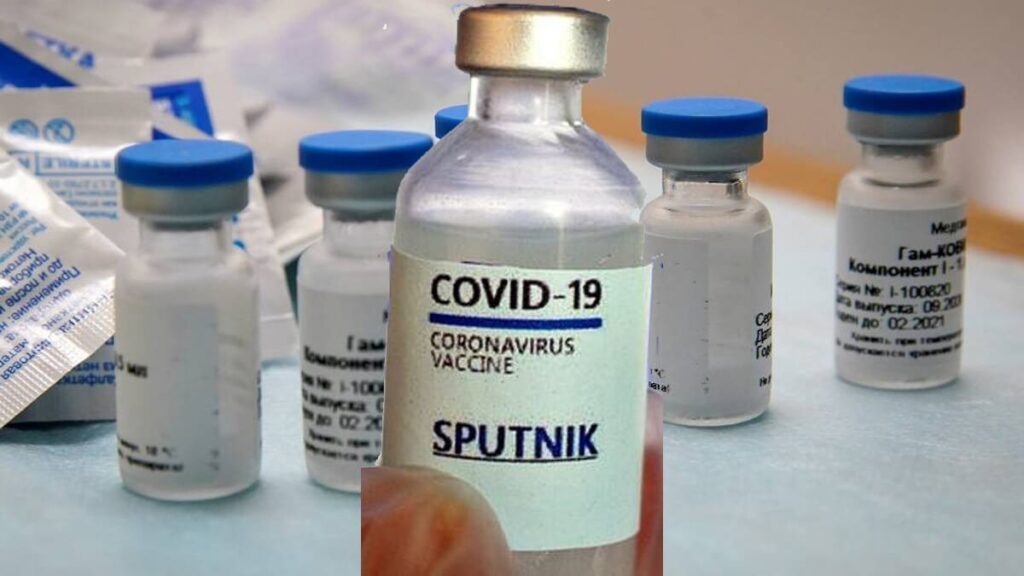
Anvisa nega importação da vacina Sputnik por falta de dados e risco de doença
De acordo com os técnicos da Anvisa, a falta de dados consistentes e problemas que colocam dúvida a segurança da vacina motivaram a decisão.
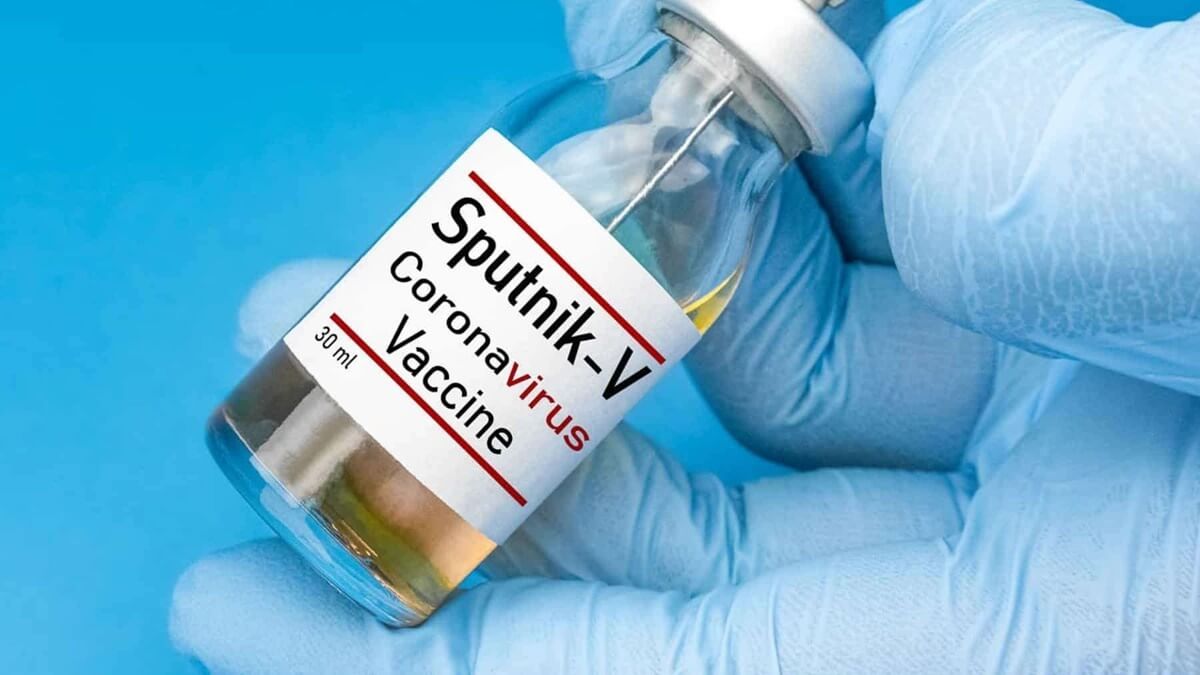
Durante uma reunião realizada nessa segunda-feira (26), a Agência Nacional de Vigilância Sanitária (Anvisa) avaliou o pedido de importação da vacina contra COVID-19 russa, a Sputnik V, desenvolvida pelo Instituto Gamaleya.
A expectativa em relação ao parecer da Anvisa era grande, uma vez que 14 estados, dentre eles a Bahia, pediram autorização para importar cerca de 30 milhões de doses desse imunizante, o que poderia acelerar o ritmo de vacinação no país.
No entanto, de acordo com a avaliação dos técnicos da Agência, a documentação necessária para a aprovação da vacina Sputnik V não possui dados consistentes. Além disso, as informações enviadas à Anvisa colocam em dúvida a eficiência e segurança desse imunizante. Por isso, a Anvisa não aprovou a importação dessa vacina.
Entenda abaixo, com detalhes, o que motivou esse decisão da Agência.
Anvisa alega falta de dados
Segundo a Anvisa, a legislação brasileira exige a entrega de um Relatório Técnico de Avaliação da Vacina, que deve ser emitido por uma autoridade sanitária internacional.
Esse documento deve mostrar que o imunizante consegue atender aos padrões de qualidade necessários para o seu uso na população. Porém, esse relatório não foi entregue.
Isso levou a Gerência Geral de Medicamentos e Produtos Biológicos, bem como a Gerente-geral de Inspeção e Fiscalização Sanitária e a Gerência Geral de Monitoramento de Produtos Sujeitos à Vigilância Sanitária se posicionarem contra a importação do imunizante.
No entanto, não foi apenas uma questão burocrática que motivou esse posicionamento.
“Não são informações burocráticas. O que a agência vem exigindo é o mínimo para a garantia da segurança população”, declarou a diretora Meiruze Freitas, que participou da reunião da Agência.
Ainda de acordo com a médica epidemiologista e vice-presidente do Instituto Sabin, dos Estados Unidos, Denise Garrett, a decisão da Anvisa foi acertada e revela seu trabalho exemplar.
“Fizeram um trabalho meticuloso e bem respaldado. Não significa que a vacina não venha a ser boa. Significa que faltam dados. A pressão não deve ser na Anvisa — deve ser no Instituto Gamaleya para enviar os dados”, declarou Denise em sua rede social.
Sputnik V pode provocar outras doenças
A vacina Sputnik V foi desenvolvida com uma tecnologia que já é utilizada há décadas, conhecida como Vetor viral não replicante. Aliás, essa é a mesma tecnologia utilizada no imunizante da vacina de Oxford/ Astrazeneca.
Em função dessa tecnologia, a vacina russa foi desenvolvida utilizando vírus inofensivos como base, que carregam uma parte do coronavírus. Ao entrar no organismo humano, após a vacinação, esses vírus inofensivos simulam o “comportamento” do SARS-CoV-2 (o vírus da COVID-19).
Dessa forma, o imunizante poderia gerar uma resposta imune no corpo, treinando o organismo para quando a ameaça real, que é o coronavírus, caso ele realmente infectasse a pessoa vacinada.
Na Sputnik V, o vírus inofensivo utilizado no seu desenvolvimento foi o adenovírus, que deveria ter sido modificado geneticamente para não conseguir se replicar, ou seja, se reproduzir, para não provocar surgimento de outra doença.
No entanto, de acordo com os técnicos da Anvisa, o adenovírus conseguem se reproduzir no organismo humano, o que não poderia acontecer de nenhuma maneira nesse tipo de vacina. Segundo Gustavo Mendes, gerente-geral de medicamentos e produtos biológicos, esse é um problema grave que pode gerar efeitos colaterais problemáticos nas pessoas que receberem esse imunizante.
“A presença de uma adenovírus replicante pode ter impacto na nossa segurança quando utilizamos essa vacina. Esse vírus, que não era para ser replicante, pode se acumular em tecidos específicos do corpo como, por exemplo, os rins”, explicou Mendes.
Ainda segundo Gustavo Mendes, essa avaliação foi possível porque a Anvisa testou a vacina em laboratório, onde detectaram que os adenovírus conseguem se multiplicar.
“Isso foi detectado em todos os lotes apresentados. Isso não foi justificado nem é aceito quando comparamos com as recomendações internacionais nem com outras vacinas de adenovírus”, disse o gerente-geral.
Anvisa não foi autorizada a inspecionar o Instituto Gamaleya
Antes de aprovar a CoronaVac, os técnicos da Anvisa viajaram até a China para realizar a inspeção do farmacêutica Sinovac, responsável pelo desenvolvimento desse imunizante. Essa etapa é fundamental para permitir que os técnicos confiram se as vacinas estão sendo produzidas com segurança sanitária.
O mesmo procedimento deveria ter sido realizado no Instituto Gamaleya, responsável pelo desenvolvimento da vacina Sputnik V. No entanto, os técnicos não receberam autorização para realizar essa inspeção.
De acordo com a Anvisa, a fabricação do imunizante russo envolve 7 fábricas. Porém, os técnicos só tiveram acesso à 3 delas. Mesmo assim, durante essas visitas foram detectados problemas de esterilidade que colocam em risco a segurança das doses.
Dúvidas sobre a eficácia da Sputnik V
Os testes da vacina russa revelaram que ela possui uma eficácia de 91,6%. No entanto, os técnicos da Anvisa questionam problemas na metodologia e na condução das análises do imunizante.
A Anvisa utiliza as orientações do Conselho Internacional de Harmonização de Requisitos Técnicos para Produtos Farmacêuticos para Uso Humano (ICH, na sigla em inglês) e da Organização Mundial da Saúde para avaliar as vacinas.
De acordo com essas orientações, os métodos utilizados durante a pesquisa do imunizante, incluindo esclarecimento sobre coleta de amostras e monitoramento de efeitos colaterais, precisam ficar claros. No entanto, isso não ocorreu em relação ao desenvolvimento da vacina russa.
“A gente sabe que as vacinas de adenovírus têm eventos de interesse especial que precisam ser monitorados. Neste caso, não vimos nenhum ser elencado, a não ser o agravamento da covid por causa da vacina. Isso faz com que a atenção que foi dada à segurança dessa vacina traga sérios problemas regulatórios”, explicou Gustavo Mendes, Gerente-geral de Medicamentos e Produtos Biológicos.
A Anvisa ainda lembrou que os resultados preliminares de eficiência da Sputnik V foram publicados na revista científica The Lancet, uma das mais respeitadas do mundo.
Contudo, Gustavo Mendes lembrou que uma avaliação sanitária é diferente de uma avaliação para aprovação de um estudo que será publicado numa revista. É diferente porque é mais complexa e exige a comprovação da eficácia da vacina.
“Uma avaliação sanitária é diferente da que é feita por uma revista científica. Uma revista científica não tem por objetivo recomendar ou não o uso de uma vacina, nem tem o compromisso de verificar boas práticas clínicas ou tem como pressuposto o acesso a todos os dados brutos e laudos”, explicou Mendes.
Mas essa vacina não foi aprovada em outros países?
De acordo com o Instituto Gamaleya, até o momento, a utilização da Sputnik V foi autorizada em 61 países. No entanto, segundo a Gerente-geral de Monitoramento de Produtos Sujeitos a Vigilância Sanitária no Brasil, Suzie Marie Gomes, dentre os 51 países consultados, somente 14 realmente estão utilizando o imunizante.
“A maior parte dos países em que houve comercialização da vacina não possui tradição em farmacovigilância”, disse Gomes.
O médico epidemiologista Paulo Lotufo, professor da Universidade de São Paulo (USP), comentou o caso e explicou que a aprovação em outros países não é garantia da segurança de uma vacina ou medicamento.
“A talidomida indicada para enjoo na gravidez nos anos 50 foi proibida em um único país, os Estados Unidos. Europa e Brasil a aprovaram e o resultado é conhecido até agora com pessoas que nasceram mutiladas. O que importa é a qualidade da avaliação, não o número de aprovações”, comentou o professor.
Seja integrante de nossos grupos de WhatsApp!
Falabarreiras Notícias 20
Falabarreiras Notícias 42
Falabarreiras Notícias 43
Seja integrante de nossos grupos de WhatsApp!
Falabarreiras Notícias 01
Falabarreiras Notícias 02
Falabarreiras Notícias 20
Falabarreiras Notícias 42
Falabarreiras Notícias 43
Falabarreiras Notícias 44
Falabarreiras Emprego 01
Falabarreiras Emprego 15
Falabarreiras Emprego 16
Falabarreiras Emprego 17
Falabarreiras Emprego 18